Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
I. BIẾT CÔNG THỨC HÓA HỌC CỦA HỢP CHẤT, HÃY XÁC ĐỊNH THÀNH PHẦN PHẦN TRĂM THEO KHỐI LƯỢNG CỦA CÁC NGUYÊN TỐ TRONG HỢP CHẤT
Ví dụ 1:
Các bước tiến hành:
Bước 1: Tìm khối lượng mol của hợp chất.
MKNO3 = 39 + 14 + (16x3) = 101 g/mol.
Bước 2: Tìm số nguyên tử của mỗi nguyên tố có trong một 1 mol phân tử chất đó.
Trong 1mol phân tử KNO3 có:
| KNO3 | K | N | O |
| 1 mol | 1 mol | 1 mol | 3 mol |
Bước 3: Tính thành phần phần trăm theo khối lượng các nguyên tố trong hợp chất.
%mK = 10139.100% = 38,6%
%mN = 10114.100% = 13,8%
%mO = 100% - (38,6 + 13,8)% = 47,6%
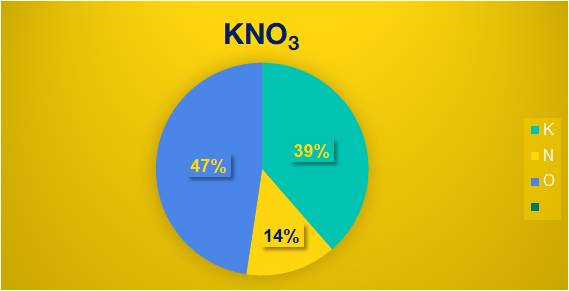
Thành phần phần trăm các nguyên tố của hợp chất KNO3.
Ví dụ 2: Một hợp chất hóa học có công thức là CaSO4, em hãy xác định thành phần phần trăm (theo khối lượng) của các nguyên tố.
Bước 1: Tìm khối lượng mol của hợp chất.
MCaSO4 = 40 + 32 + (16 x 4) = 136 g/mol.
Bước 2: Tìm số nguyên tử của mỗi nguyên tố có trong một 1 mol phân tử chất đó.
| CaSO4 | Ca | S | O |
| 1 mol | 1 mol | 1 mol | 1 mol |
Bước 3: Tính thành phần phần trăm theo khối lượng các nguyên tố trong hợp chất.
%mCa = 13640.100% = 29,4%
%mS = 13632.100% = 23,5%
%mO = 100% - (29,4 + 23,5)% = 47,1%

Thành phần phần trăm các nguyên tố của hợp chất CaSO4.
Cho biết chất nào giàu nitơ nhất trong các chất sau?
2. BIẾT THÀNH PHẦN CÁC NGUYÊN TỐ, HÃY XÁC ĐỊNH CÔNG THỨC HÓA HỌC CỦA HỢP CHẤT
Ví dụ 1:
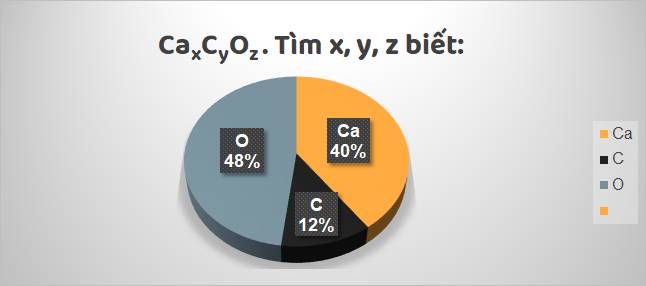
Các bước tiến hành:
| Bước 1: Tìm khối lương của mỗi nguyên tố có trong 1 mol hợp chất. | Bước 2: Tìm số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất |
mCa = 100 x 40% = 40 gam mC = 100 x 12% = 12 gam mO = 100 x 48% = 48 gam | nCa = 4040 = 1 mol nC = 1212 = 1 mol nO = 1648 = 3 mol |
⇒ Trong 1 phân tử hợp chất đó có: 1 nguyên tử Ca, 1 nguyên tử C, 3 nguyên tử O.
⇒ Công thức hóa học của hợp chất là: CaCO3.
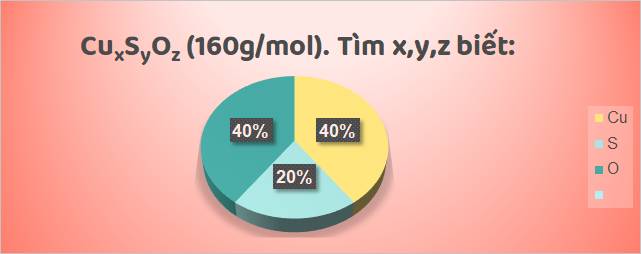
Các bước tiến hành:
| Bước 1: Tìm khối lương của mỗi nguyên tố có trong 1 mol hợp chất. | Bước 2: Tìm số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất |
mCu = 160 x 10040 = 64 gam mS = 160 x 10020 = 32 gam mO = 160 - (64 + 32) = 64 gam | nCu = 6464 = 1 mol nS = 3232 = 1 mol nO = 1664 = 4 mol |
⇒ Trong 1 phân tử hợp chất đó có: 1 nguyên tử Cu, 1 nguyên tử S, 4 nguyên tử O.
⇒ Công thức hóa học của hợp chất là: CuSO4.
Sắt oxit có tỉ số khối lượng sắt và oxi là 21 : 8. Công thức hoá học của sắt oxit đó là
Các bước tiến hành:
1. Biết công thức hóa học, tìm thành phần các nguyên tố:
Tìm khối lượng mol của hợp chất, tìm số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất → tìm thành phần theo khối lượng của mỗi nguyên tố.
2. Biết thành phần các nguyên tố, tìm công thức hóa học:
Tìm số mol nguyên tử của mỗi nguyên tố trong hợp chất → lập công thức hóa học của hợp chất.
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
Bạn có thể đăng câu hỏi về bài học này ở đây
